Estrutura de agente antitumoral é analisada com luz síncrotron
Maria Fernanda Ziegler | Agência FAPESP – Medicamentos de alta complexidade, como agentes antitumorais, podem acarretar efeitos colaterais, além de muitas vezes exigir o uso de elevadas doses. Para melhorar essas terapias e dar mais qualidade de vida aos pacientes, muitas vezes é necessário fazer análises também complexas, não só das moléculas que constituem o medicamento, mas das relações entre a sua estrutura e as propriedades físico-químicas.
Um grupo de pesquisadores conseguiu, pela primeira vez, descrever a estrutura e as interações atômicas do fármaco oncológico Lapatinib, principalmente sobre sua relação com polímeros que podem ser utilizados para a otimização do medicamento.
O estudo, publicado na Scientific Reports, utilizou raios X de alta energia, gerados por fontes de luz síncrotron no Argonne National Laboratory, nas imediações de Chicago (Estados Unidos). O trabalho, realizado na Purdue University, teve apoio da FAPESP por meio de uma Bolsa de Pesquisa no Exterior.
“O foco do estudo foi buscar informações estruturais sobre a interação entre polímeros – usados para melhorar a solubilidade e estabilizar o fármaco – e o agente antitumoral Lapatinib. Conseguimos resultados interessantes para acelerar o desenvolvimento de formulações, escolher o polímero mais apropriado e, potencialmente no futuro, também reduzir a dosagem do medicamento”, disse Gabriel Lima Barros de Araujo, primeiro autor do estudo e professor no Departamento de Farmácia da Faculdade de Ciências Farmacêuticas da Universidade de São Paulo.
O Lapatinib é um agente antitumoral oral utilizado para tratamento de câncer de mama metastático ou avançado. Ele integra a classe de medicamentos conhecidos como pequenas moléculas inibidoras da tirosina-quinase, que atua inibindo sinalizadores da cascata de expressão de proliferação celular.
“Essa é uma das terapias orais mais específicas que existem, porém apresenta muita variabilidade na resposta clínica e, geralmente, os pacientes precisam tomar doses elevadas do medicamento, cerca de seis comprimidos por dia. Além disso, sabe-se que, em muitos casos, a alimentação pode interferir na absorção desse fármaco, ocasionando efeitos adversos. Uma das alternativas é melhorar as formulações”, disse Araujo.
No estudo, além da estratégia de extração de interações intermoleculares a partir do uso de raios X de alta energia – que mostrou que as moléculas de Lapatinib não se aglomeram da mesma maneira observada em técnicas anteriores –, os pesquisadores usaram também uma técnica diferente de análise.
“Tratamos os dados com uma metodologia chamada de ‘função de distribuição de pares’, que permite avaliar a distância entre os pares de átomos, o que nos forneceu muitas informações sobre as interações intermoleculares do agente antitumoral com os polímeros”, disse Araujo.
Sistemas amorfos
Entender como as interações ocorrem é essencial para a melhora da formulação. No entanto, nesse trabalho a análise do Lapatinib se tornou mais complexa pelo fato de ele fazer parte das chamadas “dispersões sólidas amorfas”, sistemas instáveis formados a partir da dissolução dos cristais do fármaco e pela dispersão de suas moléculas em polímeros, o que aumenta a solubilidade e, consequentemente, pode promover a melhoria na sua absorção pela via oral de administração.
“Para que ele se tornasse estável, foram feitas ligações iônicas entre o fármaco e o polímero. No entanto, são sistemas dificílimos de serem estudados por serem desorganizados, não possuindo uma estrutura definida”, disse Araujo.
Segundo ele, para superar a baixa solubilidade e melhorar o aproveitamento de fármacos como os antitumorais, tem crescido a investigação de sistemas amorfos e nanocristalinos, como é o caso do Lapatinib.
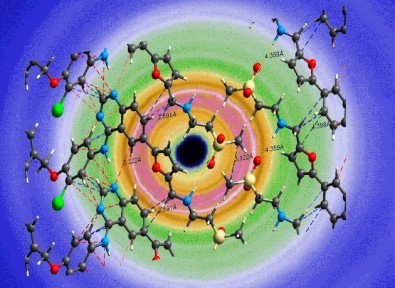
Também tem aumentado a busca por métodos para caracterizar a interação átomo a átomo em sistemas amorfos formados por fármacos e polímeros. Nos sistemas amorfos, os átomos são ordenados principalmente a distâncias curtas (de 2 a 5 angstroms – décimo do bilionésimo do metro) e médias (de 5 a 20 angstroms), o que torna a determinação da estrutura atômica uma tarefa desafiadora, que não pode ser abordada pela cristalografia clássica.
A utilização de raios X de alta energia produzidos pela luz síncrotron permitiu o uso de comprimentos de onda curtos, um pré-requisito para aumentar a resolução do espaço real e obter dados mais precisos.
A expectativa é que outros princípios ativos também passem pela mesma análise do grupo de pesquisadores. “Em 2017, junto com Chris Benmore, do Argonne National Laboratory, e Stephen Byrn, professor em Purdue, iniciamos outros trabalhos a partir desse estudo. Nossa intenção é continuar com a parceria e analisar outros medicamentos futuramente”, disse Araujo.
O artigo Local Structure of Ion Pair Interaction in Lapatinib Amorphous Dispersions characterized by Synchrotron X-Ray diffraction and Pair Distribution Function Analysis (doi: 10.1038/srep46367), de Gabriel L. B. de Araujo, Chris J. Benmore e Stephen R. Byrn, pode ser lido na Scientific Reports em www.nature.com/articles/srep46367.
